Quando pensiamo ai metalli nobili come oro, argento e platino, spesso li associamo a gioielli e tesori. Ma cosa li rende così preziosi anche al di là del loro splendore? In questo articolo, esploreremo le straordinarie proprietà di questi metalli che non solo resistono alla corrosione e all’ossidazione ma presentano anche interessanti fenomeni come gli effetti relativistici. Scopriamo perché questi metalli sono veramente ‘nobili‘ nel mondo della scienza. 💎
Cosa Sono i Metalli Nobili?
Rutenio, rodio, palladio, argento, osmio, iridio, platino e oro rappresentano un gruppo particolarmente prestigioso tra gli elementi chimici, comunemente noti come metalli nobili. Questi metalli si distinguono per le loro eccezionali proprietà di resistenza alla corrosione e all’ossidazione, caratteristiche che mantengono invariabilmente anche ad alte temperature. La loro notevole resistenza agli attacchi chimici, inclusi quelli degli acidi, conferisce loro un valore inestimabile in numerosi campi applicativi.
Proprietà Uniche e Applicazioni
- Dal punto di vista chimico, i metalli nobili sono particolarmente stabili. Non reagiscono facilmente con altri elementi e mantengono la loro lucentezza e struttura anche quando esposti a ambienti severi. Questa caratteristica li rende ideali per applicazioni in cui la purezza e la durata sono essenziali.
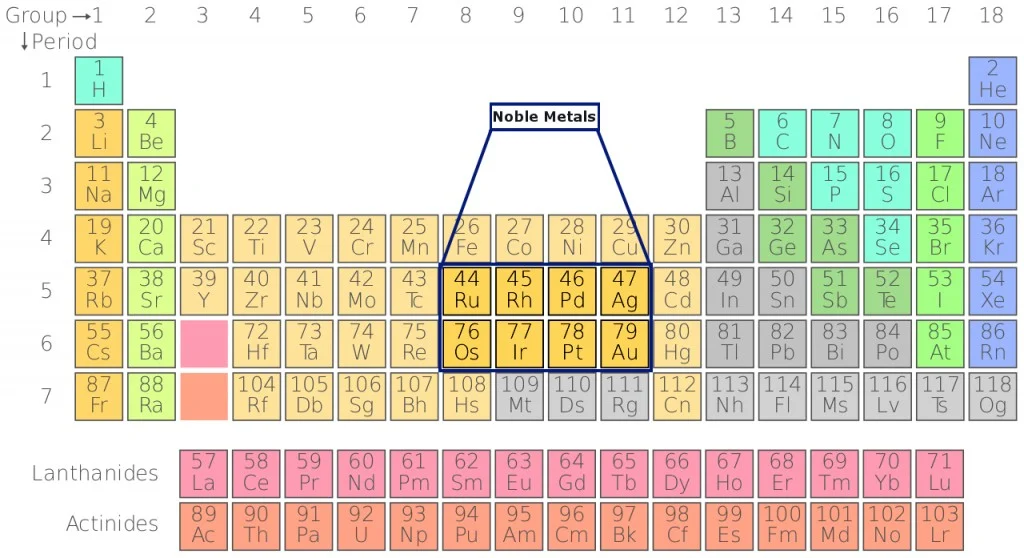
- Fisicamente, il termine ‘metalli nobili‘ si riferisce a elementi come il rame, l’argento e l’oro, noti per le loro shell di valenza $d$ complete che contribuiscono alla loro eccellente conduttività elettrica. Questi metalli non solo conducono elettricità con efficienza, ma sono anche altamente duttili e malleabili, il che li rende perfetti per la lavorazione industriale e artistica. Si discute se includere zinco, cadmio e mercurio in questo gruppo. Il mercurio è particolarmente notevole essendo l’unico metallo che rimane liquido a temperatura ambiente.
Generalmente, i metalli nobili sono considerati stabili e minimamente reattivi, tendendo a non formare composti chimici con facilità. Tuttavia, la configurazione elettronica degli elementi del gruppo 11, che include metalli nobili dal punto di vista fisico, presenta una peculiarità interessante.
Questi elementi possiedono un elettrone nella shell $s$ esterna, che è libero di muoversi all’interno del materiale quando è esposto a un campo elettrico. Questa libertà di movimento è fondamentale per le loro proprietà di conduttività elettrica superiore e contribuisce significativamente alla loro efficienza come conduttori.
Nobiltà Elettrochimica dei Metalli
La serie elettrochimica è un elenco di elementi chimici ordinati in base al loro potenziale standard di riduzione, che indica la loro tendenza a guadagnare elettroni e quindi la loro capacità di agire come agenti riducenti o ossidanti.
Nella serie elettrochimica, metalli come oro, argento e rame sono posizionati sopra l’idrogeno, segnalando la loro forte capacità ossidante e la loro riluttanza a cedere elettroni. Unicamente, l’oro si trova anche al di sopra dell’ossigeno, suggerendo che, a differenza di argento e rame, è ancora più restio a cedere il suo elettrone più esterno.

Questa caratteristica è parzialmente influenzata dagli effetti relativistici, che diventano rilevanti a partire dal sesto periodo della tavola periodica con l’introduzione degli orbitali di tipo $f$.
Contrazione dei Lantanoidi e Effetti sui Metalli Transizionali
Il fenomeno noto come contrazione dei lantanoidi inizia con il lantanio, elemento numero 57, e continua fino al lutezio, numero 71. Questa contrazione influenza non solo i lantanoidi stessi ma estende il suo impatto anche agli attinidi e ai metalli di transizione successivi, come l’oro, contribuendo alla stabilità chimica e alla minore reattività che sono caratteristiche distintive dei metalli nobili.
La causa di questa contrazione è attribuita alla diffusione degli orbitali $f$, che sono meno efficaci nel schermare l’attrazione coulombiana tra il nucleo e gli orbitali più esterni, come quelli $5d$ e $6s$. Gli effetti relativistici, che si intensificano con l’aumentare delle dimensioni atomiche, giocano anch’essi un ruolo significativo.
La contrazione dei lantanoidi è il fenomeno per cui il raggio atomico degli elementi del gruppo dei lantanoidi diminuisce progressivamente lungo la serie a causa dell’inefficace schermatura degli elettroni $f$ interni, che aumenta l’attrazione tra gli elettroni di valenza e il nucleo.
Effetti Relativistici sui Metalli Pesanti
Gli effetti relativistici sono particolarmente evidenti nei metalli nobili pesanti, come l’oro. Più grande è l’atomo, maggiore è il numero di protoni nel nucleo e di elettroni, e maggiore è la reciproca attrazione coulombiana. Per evitare di cadere nel nucleo, gli elettroni sono costretti a viaggiare a velocità relativistiche, a qualche frazione di c (costante che indica la velocità della luce nel vuoto). Di conseguenza, per via della relazione di Einstein fra massa ed energia valida a regimi relativistici, la massa elettronica aumenta.
In particolare, per costruzione: gli orbitali s e p hanno probabilità maggiore di avere gli elettroni vicino al nucleo, mentre gli orbitali d ed f hanno probabilità maggiore di avere gli elettroni lontano dal nucleo. Questo significa che tutti gli orbitali di tipo s e p si contraggono verso il nucleo, portandosi ad un livello energetico più basso. Così facendo si legano ancora più fortemente ad esso schermano l’attrazione coulombiana verso gli orbitali più esterni. Gli orbitali d ed f, invece, si espandono allontanandosi dal nucleo, proprio perché quelli più interni ne schermano la attrazione e si portano, quindi, ad un livello di energia superiore
Tutto questo fa diminuire il raggio atomico dei metalli pesanti essendo questi determinato dalla posizione della nuvola elettronica corrispondente all’orbitale $s$ più esterno che si contrae.
Il Principato dell’Oro
L’oro, con il suo numero atomico di 79, è fortemente influenzato dagli effetti relativistici. Questi causano una contrazione dell’orbitale più esterno, rendendo l’elettrone della shell $s$ esterna, meno disponibile per formare legami chimici. Questa peculiarità contribuisce a rendere l’oro estremamente stabile e meno reattivo, una delle ragioni per cui è classificato come metallo nobile.